聚焦骨类器官与器官芯片,苏佳灿教授团队连发11篇高质量论文
2024-05-28 文章来源:上海交通大学医学院附属新华医院骨科 作者:苏佳灿教授团队 我要说
近期,上海交通大学医学院附属新华医院骨科/上海大学转化医学研究院苏佳灿教授团队依托国家重点研发计划、国家自然科学基金重点项目、重大研究计划集成项目,围绕骨类器官构建、DNA骨类器官水凝胶基质开发和人工智能技术指导骨类器官研究,在国际高影响力期刊上连续发表11篇高质量学术论文,分别发表于Advanced Materials、Bioactive Materials、Small、Materials Horizons等杂志,其中IF最高29.4分。
团队主要围绕骨和软骨类器官DNA水凝胶基质材料开发,骨和软骨类器官生物活性3D打印支架开发,骨和软骨类器官干细胞筛选和研究,构建1.0版本骨和软骨类器官,实现体外骨和软骨的三维大尺度长期培养,为未来骨/软骨类器官应用于体外模拟、药物筛选和组织再生奠定坚实基础。
1.骨类器官新视野:构建与应用展望
Chen S, Chen X, Geng Z, Su J. The horizon of bone organoid: A perspective on construction and application. Bioact Mater. 2022 Feb 5;18:15-25. doi: 10.1016/j.bioactmat.2022.01.048. PMID: 35387160; PMCID: PMC8961298.
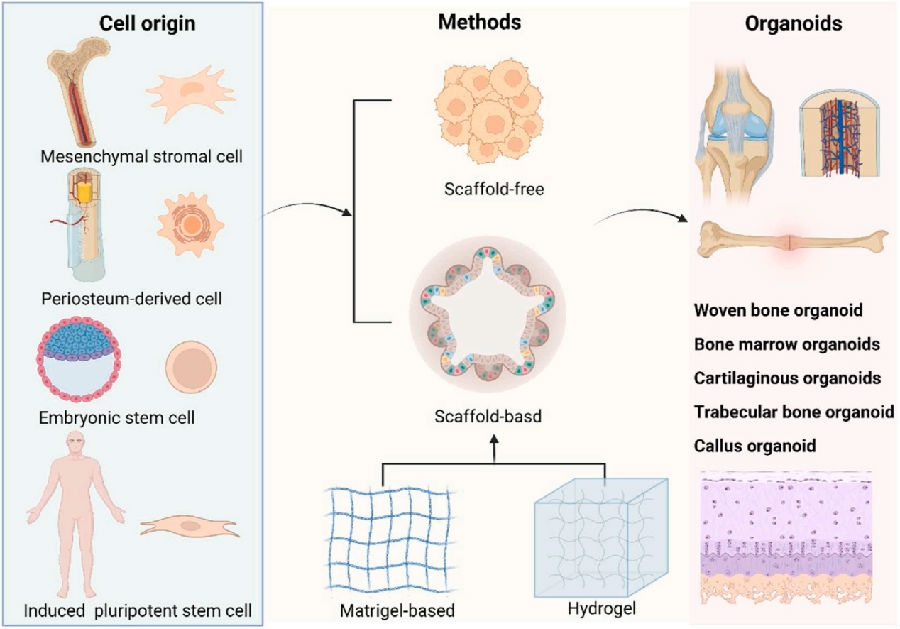
2022年团队首次提出骨类器官概念,即通过组织工程技术和生物活性材料的应用,可以在体外构建能够模拟真实器官复杂生物功能的体外培养物。这种新兴的研究领域弥补传统二维细胞培养和动物实验模型的不足,为个性化医疗和精准治疗提供新的研究工具。
文章全面审视骨类器官的构建与应用前景,突出了生物活性材料在调控干细胞命运中的关键作用,以及通过组织工程技术基于生物理论构建的体外类器官如何模拟体内器官的复杂生物功能。骨类器官作为一种新的概念,其研究和应用前景在器官发育、药物筛查和机理研究等多个方面显示出广泛应用潜力。
本综述介绍了骨微环境特点和类器官概念,着重讨论了骨类器官研究进展,提出了骨类器官构建的策略、研究方向和应用前景。这项工作为个性化医疗研究反映复杂器官样生理微环境提供了理想模型,体现了团队在骨类器官工程领域的领导地位和学术贡献。
(文章链接:https://www.sciencedirect.com/science/article/pii/S2452199X22000652)
2.骨类器官1.0版本——骨基质启发的羟基磷灰石杂化生物墨水用于生物打印构建大尺寸骨类器官
Wang J, Wu Y, Li G, Zhou F, Wu X, Wang M, Liu X, Tang H, Bai L, Geng Z, Song P, Shi Z, Ren X, Su J. Engineering Large-Scale Self-Mineralizing Bone Organoids with Bone Matrix-Inspired Hydroxyapatite Hybrid Bioinks. Adv Mater. 2024 Apr 20:e2309875. doi: 10.1002/adma.202309875. Epub ahead of print. PMID: 38642033.
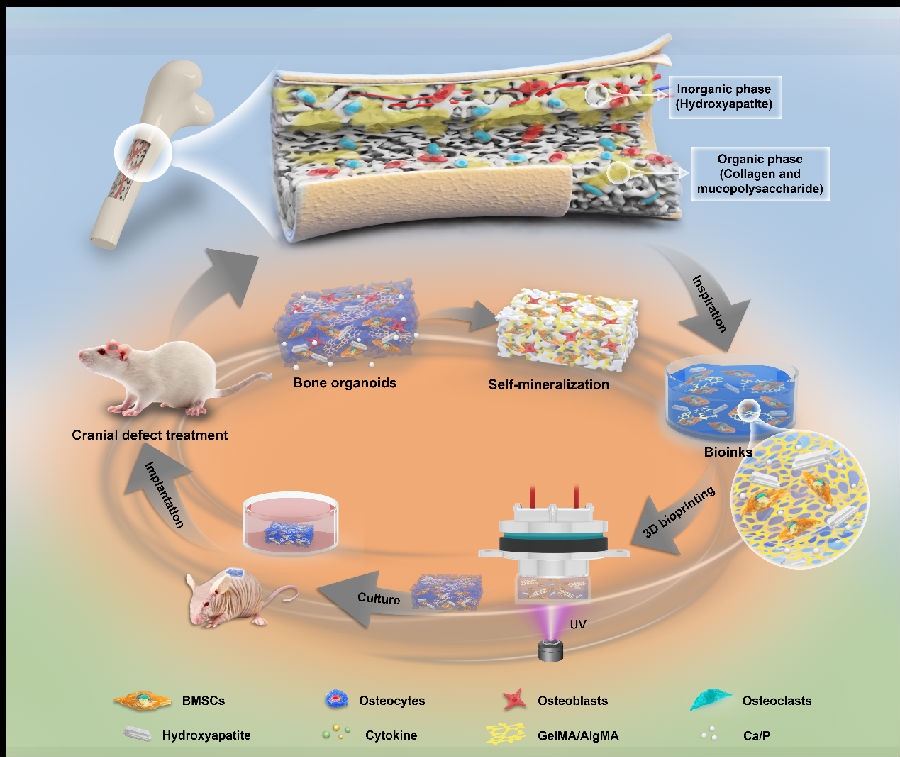
由于临界骨缺损骨自愈能力有限,目前临床上大段骨缺损修复仍面临巨大挑战。高活性功能化骨类器官为解决这一临床难题提供了新策略。骨类器官是基于生物活性材料、利用干细胞或祖细胞定向分化、能够自我更新和自组织、具有仿生三维空间特征微骨组织,在形态和功能上与原生组织相似,为骨组织工程提供了新解决方案。
研究人员通过设计全新适用骨组织工程的生物墨水,利用数字光处理生物打印技术,精确复制骨组织复杂微观结构,在体内外长时间的定向培育,分化成含有多种骨髓细胞(血细胞、免疫细胞、血管内皮细胞、软骨细胞、成骨细胞,脂肪细胞和破骨细胞),力学性能良好(杨氏模量MPa级,接近于松质骨),空间拓扑结构类骨(疏松多孔的微纳结构)和大尺寸(厘米级)的功能性骨cx器官,应用于骨缺损模型的再生修复,显示出强大的修复能力。
(文章链接:https://onlinelibrary.wiley.com/doi/abs/10.1002/adma.202309875)
3.构建基于丝素蛋白-DNA水凝胶的初代软骨类器官促进软骨修复研究
C.Shen, J. Wang, G. Li, S. Hao, Y. Wu, P. Song, Y. Han, M. Li, G. Wang, K. Xu, H. Zhang, X. Ren, Y. Jing, R. Yang, Z. Geng, J. Su, Boosting cartilage repair with silk fibroin-DNA hydrogel-based cartilage organoid precursor, Bioact. Mater., 35 (2024) 429-444. doi: 10.1016/j.bioactmat.2024.02.016
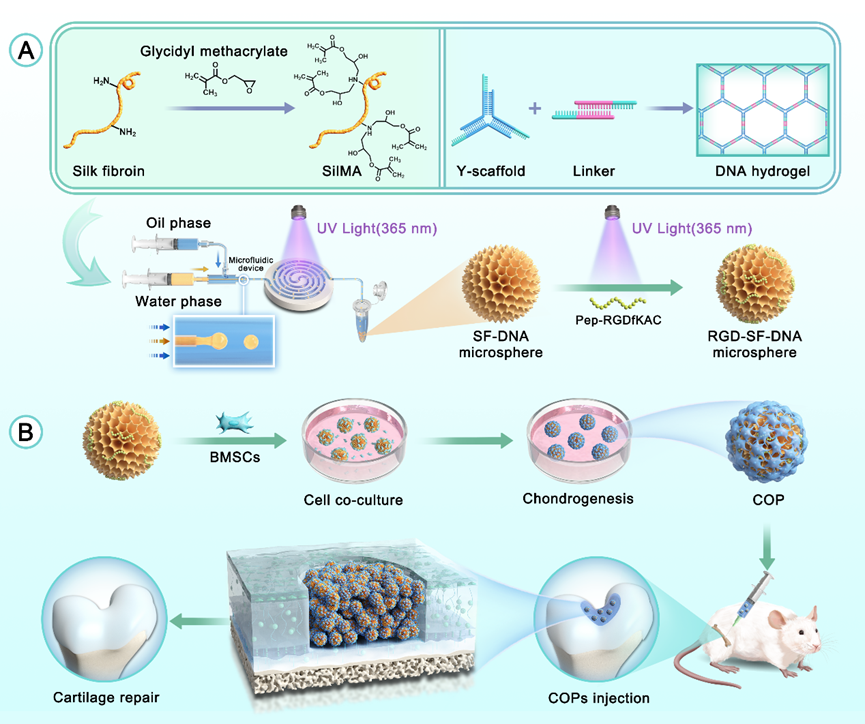
骨关节炎(OA)的软骨修复一直是临床挑战,现有治疗手段无法有效促进关节软骨修复。近期研究焦点转向了体外培养软骨类器官,其不仅能够模拟天然软骨功能,还能促进宿主组织修复,为软骨组织工程和再生医学领域提供了创新策略。团队使用光交联与自组装技术的微流控集成系统制备新型RGD-丝素蛋白-DNA水凝胶微球(RSD-MS)并基于此构建初代软骨类器官。RSD-MS具有均一粒径分布、良好溶胀性能和适宜降解性。RSD-MS可以上调整合素介导的细胞黏附和局部黏附通路,从而促进糖胺聚糖的生物合成,诱导BMSCs成软骨分化。最后,将RSD-MS和COP植入SD大鼠软骨缺损模型中进行软骨修复功能验证,可显著加速软骨再生修复。RSD-MS作为一种构建和长期培养软骨类器官理想材料,为软骨类器官构建提供了一种创新策略。
(文章链接:https://www.sciencedirect.com/science/article/pii/S2452199X24000616)
4.异质DNA水凝胶负载Apt02修饰的四面体框架核酸加速临界尺寸骨缺损修复
Han Y, Wu Y, Wang F, Li G, Wang J, Wu X, Deng A, Ren X, Wang X, Gao J, Shi Z, Bai L, Su J. Heterogeneous DNA hydrogel loaded with Apt02 modified tetrahedral framework nucleic acid accelerated critical-size bone defect repair. Bioact Mater. 2024 Jan 18;35:1-16. doi: 10.1016/j.bioactmat.2024.01.009.

骨缺损常常由创伤、感染、肿瘤等原因引起,骨缺损的修复尤其是大节段骨缺损一直是骨科医生面临的重大挑战。传统的治疗方法,自体骨移植治疗骨缺损具有显着效果,但因患者自体骨来源有限而受到限制;同样异体骨移植也存在免疫排斥和疾病传播等各种风险。
近年来,新兴骨组织工程为大节段骨缺损治疗开辟了新方向。团队开发了一种新型基于核酸水凝胶以丙烯酰胺聚合物作为主链,DNA交联剂作为侧链,通过碱基互补配对形成DNA聚合物。使用64种不同DNA单链作为交联剂可以形成均匀水凝胶。交联剂互补短链使得能够在37℃自组装,适合包载细胞,显著降低传统DNA水凝胶生产成本。肌动蛋白可减缓其降解,适合长期骨修复应用。Apt02-tFNA物理混合进DNA水凝胶中赋予DNA水凝胶更优血管生成和成骨矿化能力。本研究通过构建一种新型基于核酸DNA水凝胶,为骨快速再生提供生物相容性材料,为骨缺损临床治疗和进一步构建骨类器官提供参考。
(文章链接:https://www.sciencedirect.com/science/article/pii/S2452199X24000094)
5.软骨类器官水凝胶——双链DNA丝素蛋白水凝胶调控成软骨分化
Zhou Z, Song P, Wu Y, Wang M, Shen C, Ma Z, Ren X, Wang X, Chen X, Hu Y, Li Z, Zhang Q, Li M, Geng Z, Su J. Dual-network DNA-silk fibroin hydrogels with controllable surface rigidity for regulating chondrogenic differentiation. Mater Horiz. 2024 Jan 03; 11: 1465–1483. doi: 10.1039/d3mh01581e.
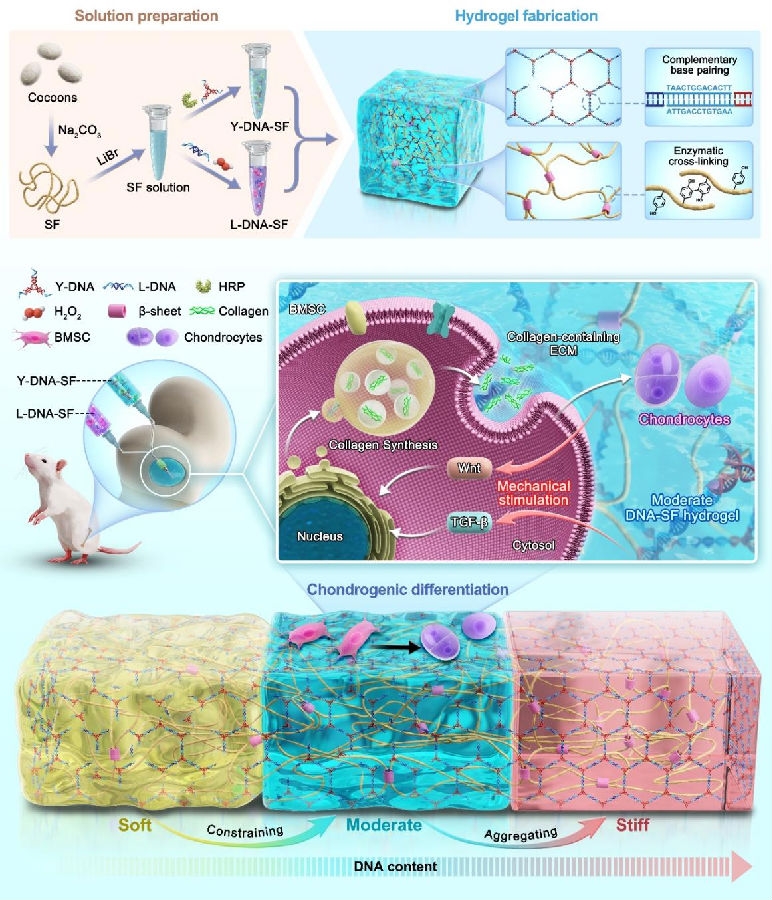
骨关节炎(OA)是一种常见关节疾病,以软骨退变为主要特征,发病率高、致残率高,给个人和社会带来巨大负担。然而,由于软骨再生机制尚不清楚,软骨再生修复一直是临床治疗难题。基于此,团队首次将DNA与丝素蛋白结合在一起制备了具备可控表面刚度的双网络DNA-丝素蛋白水凝胶用于调控干细胞成软骨分化。其中,DNA通过碱基互补配对形成DNA超分子网络,诱导SF分子形成β-折叠进而调控水凝胶表面刚度;此外,实验表明具备适中表面刚度双网络DNA-丝素蛋白水凝胶利于BMSCs成软骨分化。具备适中表面刚度双网络DNA-丝素蛋白水凝胶可以上调BMSCs Wnt信号通路和TGF-β信号通路,促进含胶原的细胞外基质分泌,加速关节软骨缺损修复。
(文章链接:https://pubs.rsc.org/en/content/articlelanding/2024/mh/d3mh01581e)
6.小关节类器官:构建策略与应用
Zhang Y, Li G, Wang J, Zhou F, Ren X, Su J. Small Joint Organoids 3D Bioprinting: Construction Strategy and Application. Small. 2024 Feb;20(8):e2302506. doi: 10.1002/smll.202302506. Epub 2023 Oct 9. PMID: 37814373.

3D生物打印通过模仿发育生物学途径,能够设计紧密模仿关节解剖几何形状的多层组织结构,可以最大程度地恢复体内微环境。此外,由于其空间特性和机械结构,通过3D生物打印技术构建关节类器官,可以承受植入关节中存在的高水平压缩和剪切载荷。理想的骨软骨组织应该像天然骨软骨组织一样作为具有ECM梯度的单一结构原位生成。可合成的梯度,如连续材料,细胞密度,生长因子浓度,水凝胶刚度和孔隙率梯度,可以使用具有微流体混合器的生物打印系统产生。
本文总结了近年来用于软骨修复3D打印水凝胶支架,根据关节结构特点,提出利用3D生物打印构建模拟天然骨软骨界面的关节类器官策略,并详细描述构建具有ECM梯度、孔隙率梯度和机械梯度关节类器官。提出构建基础关节类器官策略、结构化关节类器官策略和功能化关节类器官策略三部曲。
(文章链接:https://onlinelibrary.wiley.com/doi/10.1002/smll.202302506)
7.软骨类器官水凝胶研究进展
Li X, Sheng S, Li G, Hu Y, Zhou F, Geng Z, Su J. Research Progress in Hydrogels for Cartilage Organoids. Advanced Healthcare Materials. 2024 May 20; e2400431. doi: 0.1002/adhm.202400431.

软骨修复和再生一直是医学研究热门话题。软骨类器官是使用体外组织工程技术构建的特殊软骨组织。这些工程类器官组织提供了模拟软骨复杂生物学功能模型,为软骨再生医学和治疗策略开辟了新可能。建立合适基质支架来培养软骨软骨类器官至关重要。近年来,利用水凝胶培养干细胞并诱导其分化为软骨细胞成为体外构建软骨类器官重要方法。
本研究总结建立软骨类器官方法,概述使用基质胶软骨类器官的优点和局限性,讨论基质胶的替代品-水凝胶(如海藻酸盐、肽、丝素蛋白和DNA)的重要性,阐述使用这些水凝胶培养软骨类器官的利弊。最后,本论文讨论了软骨类器官水凝胶未来的挑战和研究方向。
(文章链接:https://onlinelibrary.wiley.com/doi/abs/10.1002/adhm.202400431)
8.人工智能驱动的类器官构建、分析与应用
Bai L, Wu Y, Li G, Zhang W, Zhang H, Su J. AI-enabled organoids: Construction, analysis, and application. Bioact Mater. 2023 Sep 16;31:525-548. doi: 10.1016/j.bioactmat.2023.09.005 PMID: 37746662 PMCID: PMC10511344
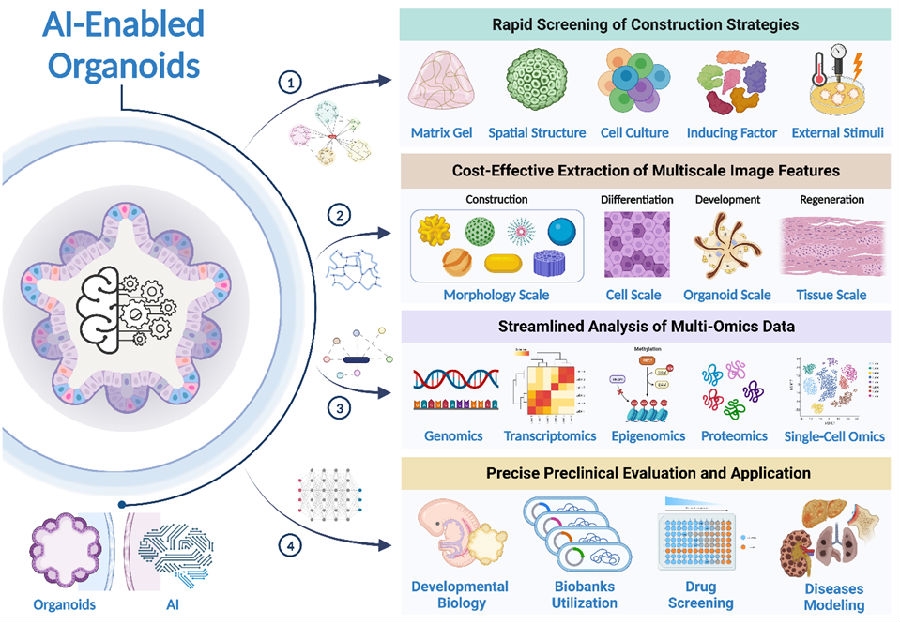
引入人工智能(AI)技术,推动AI-辅助类器官构建、分析和应用,大幅提升类器官构建的效率和质量,展现出独特优势和长远前景。通过快速筛选构建策略,AI帮助优化类器官的实验设计和实施策略,提高了构建效率和精度;在多尺度图像特征的成本效益提取方面,AI技术从多个层次和视角深入理解类器官的结构和功能;AI在多组学数据的流线型分析中发挥重要作用,有助于全面解析类器官基因表达、蛋白质组学和代谢组学等复杂数据;在临床前评价和应用方面,AI预测模型和优化算法用于评估类器官干预机制、筛选潜在药物以及构建体外疾病模型,大大提升效率和有效性。AI-辅助类器官研究为我们提供了更深入理解器官发育和疾病进展的新视角,并为未来临床应用奠定了坚实基础。这项研究展示了团队在骨类器官开发和应用中的领导地位。
(文章链接:https://www.sciencedirect.com/science/article/pii/S2452199X23002761)
9.理想的软骨类器官构建体系:DNA水凝胶载细胞外囊泡
Ma Z, Wu Y, Li G, Liu J, Geng Z, Su J. Extracellular vesicles-loaded DNA hydrogels: A promising candidate for cartilage organoids engineering. Chemical Engineering Journal. 2023 Dec 1; 477; 147146. https://doi.org/10.1016/j.cej.2023.147146
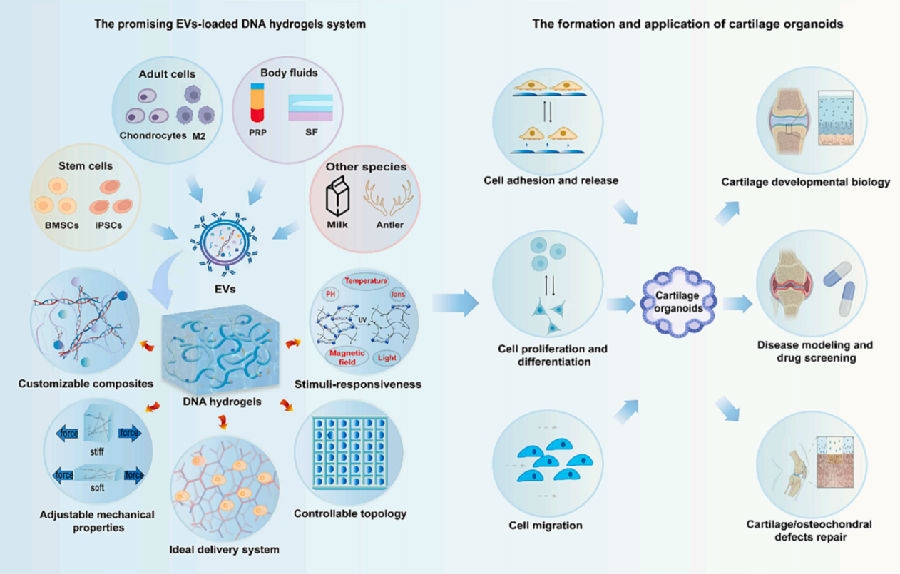
骨关节炎一直是严重威胁全球人类健康的公共卫生问题。课题组在利用外泌体负载DNA水凝胶构建软骨类器官方面取得了显著学术突破,开创性地提出了一种新型软骨组织工程策略,为软骨再生医学带来了全新视角。
DNA基水凝胶具有良好生物相容性、生物降解性、智能可编程性以及高度细胞亲和力,将外泌体与DNA水凝胶结合能够精确调控水凝胶化学成分、机械性能和空间结构,从而构建出理想三维微环境,促进细胞自组织和软骨类器官形成。这一创新性方法大幅提升了软骨类器官构建效率和质量,展现了在软骨发育研究、疾病模型建立以及药物筛选中的巨大潜力。外泌体作为多功能生物活性成分,通过多种机制显著促进软骨再生,进一步增强软骨类器官的构建效果。研究为深入理解软骨发育和病理机制提供了有力工具,为软骨缺损修复和再生治疗开辟了新应用前景。
(文章链接:https://www.sciencedirect.com/science/article/abs/pii/S1385894723058771)
10.骨/软骨类器官芯片:构建策略及应用
Hu Y, Zhang H, Wang S, Cao L, Zhou F, Jing Y, Su J. Bone/cartilage organoid on-chip: Construction strategy and application. Bioact Mater. 2023 Jan 20;25:29-41. doi: 10.1016/j.bioactmat.2023.01.016. PMID: 37056252; PMCID: PMC10087111.
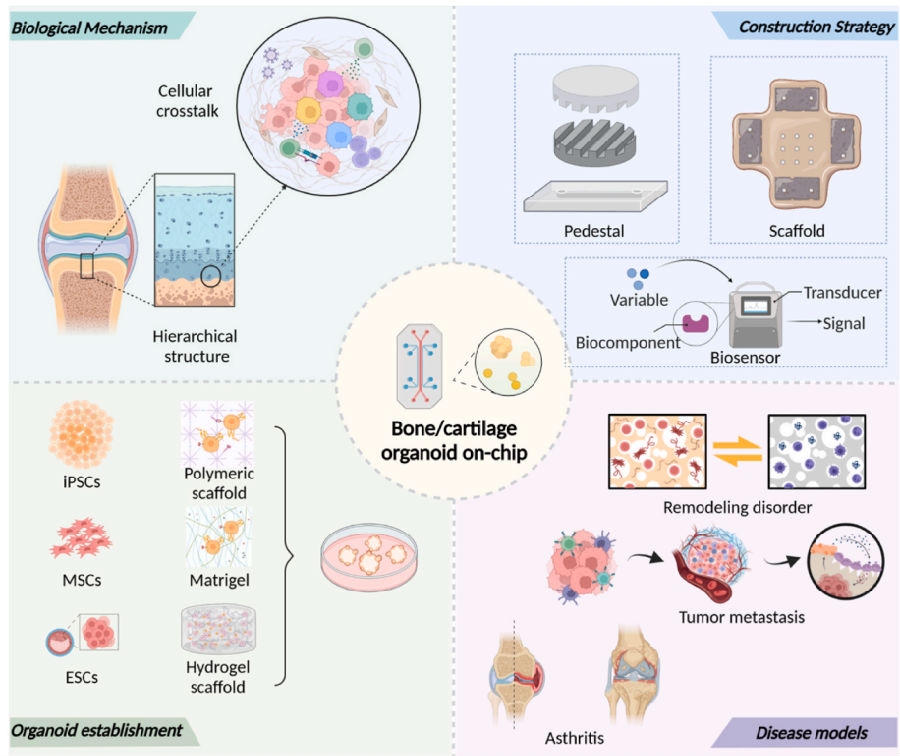
在骨软骨类器官芯片技术的研究领域,团队总结骨/软骨类器官芯片构建应用,为骨病和软骨相关疾病基础研究及药物筛选带来了突破性进展。通过精确模拟生物功能和病理响应,骨软骨类器官芯片(BCoC)系统为疾病模型提供了一种新多组织平台,极大缩小了体外细胞培养、动物模型与真实人体间的差距。研发BCoC平台模块并整合到单一微流控系统中,模拟真实情况下的基本元素、生物功能和病理生理反应是BCoC核心发展方向。团队正研究开发一系列BCoC解决现有疾病模型中的未解决问题,为在临床前评估、个性化药物开发以及精准医疗中发挥重要作用,为骨科疾病和软骨损伤治疗带来革命性改变。
(文章链接:https://www.sciencedirect.com/science/article/pii/S2452199X23000166)
11.类器官评估技术
Gu Y, Zhang W, Wu X, Zhang Y, Xu K, Su J. Organoid assessment technologies. Clin Transl Med. 2023 Dec;13(12):e1499. doi: 10.1002/ctm2.1499. PMID: 38115706; PMCID: PMC10731122.

尽管在类器官的构建已取得进展,但高效稳定地评估类器官仍是重大挑战,评估类器官结构及功能受到通量限制,需要进一步提升效率。团队总结了类器官评估技术进展,这些新技术用于鉴定和分析类器官的稳定性和真实性,涵盖了从机制研究到类器官功能评估的全面方法。
与活体人类器官/组织进行比较,强调了单细胞技术和功能属性技术在宏观和微观层面评估类器官的重要性。利用多组学分析和单细胞分析,解码细胞与细胞之间的交互作用机制,并通过组织学分析详细调查了它们的结构,为未来功能分析的发展奠定了基础,并将促进类器官成熟为模型。
高通量的筛选和多层次的分析加强了类器官在临床前评估和个性化医疗中类器官模型的评估精确度,拥有巨大的应用潜力。这些创新性的进展显著提升类器官技术的研究和应用水平,也为未来类器官成为成熟的体外研究模疾病模型提供强有力支持。
(文章链接:https://onlinelibrary.wiley.com/doi/10.1002/ctm2.1499)


 京公网安备11010502051256号
京公网安备11010502051256号